Le développement et les différents types de vaccins
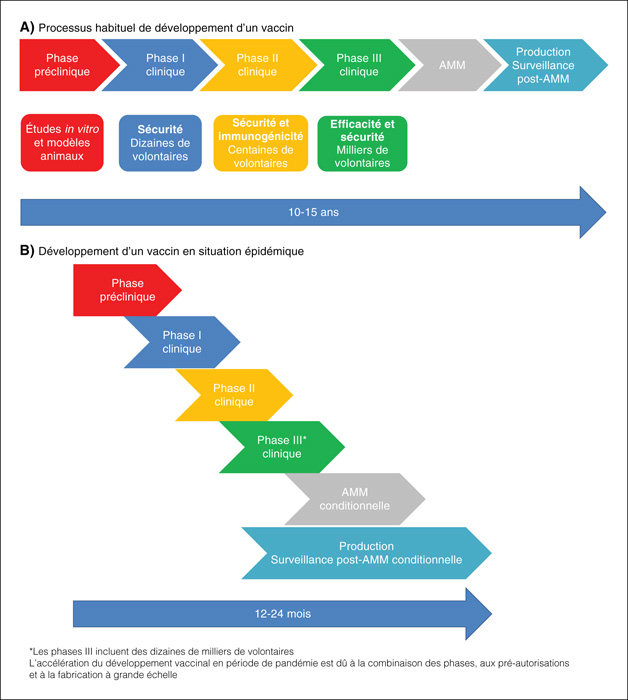
Le développement d'un vaccin comprend différentes phases :
LES TESTS PRÉCLINIQUES
Les scientifiques testent un nouveau vaccin sur des cellules et l'administrent ensuite à des animaux tels que des souris ou des singes pour voir s'il produit une réponse immunitaire.
PHASE 1 : LES ESSAIS DE SÉCURITÉ
Les scientifiques administrent le vaccin à un petit nombre de personnes pour en tester l'innocuité et le dosage, ainsi que pour confirmer qu'il stimule le système immunitaire chez l'Homme.
PHASE 2 : LES ESSAIS ÉLARGIS
Les scientifiques administrent le vaccin à des centaines de personnes réparties en groupes, tels que les enfants et les personnes âgées, pour voir si le vaccin agit différemment chez eux. Ces essais
permettent de tester davantage la sécurité du vaccin.
PHASE 3 : LES ESSAIS D'EFFICACITÉ
Les scientifiques administrent le vaccin à des milliers de personnes et attendent de voir combien d'entre elles sont infectées, par rapport aux volontaires qui ont reçu un placebo. Ces essais permettent
de déterminer si le vaccin protège contre le SARS-CoV-2, en mesurant ce que l'on appelle le taux d'efficacité. Les essais de la phase 3 sont également suffisamment importants pour révéler des preuves d'effets secondaires relativement
rares.
Les phases précliniques et les phases I et II sont réalisées en laboratoire : on mesure la quantité d’anticorps produits (totaux et neutralisants) ainsi que la réponse immunitaire cellulaire. Ces mêmes données sont évaluées tout au long de la phase III mais s’y ajoute comme mentionné ci-dessus, l’efficacité clinique à savoir le nombre de personnes infectées dans chaque groupe.
Dès le 5 janvier 2020, le génome du virus SarsCov2 a été séquencé. Ces informations ont permis aux chercheurs et aux laboratoires pharmaceutiques de se mettre rapidement à travailler à des pistes pour les vaccins.
De plus, les différentes phases du développement d'un vaccin prennent habituellement plusieurs années. Face à la situation sanitaire exceptionnelle, des autorisations ont permis de faire chevaucher les différentes phases afin d'accélérer le développement des vaccins. Par exemple, les essais cliniques de phase 1 chez l'homme ont débuté alors même que les essais chez l'animal n'étaient pas clôturés.
De plus, les essais cliniques menés par les laboratoires pharmaceutiques ne sont pas terminés. Avec la procédure standard, il aurait fallu que la période de suivi de 2 ans soit achevée avant d'obtenir une autorisation de commercialisation. Les données de suivi à quelques mois étant rassurantes, les autorités sanitaires ont décidé d'autoriser l'utilisation des vaccins dans la population générale avant la fin des essais cliniques. Pour autant, la surveillance sera effective pendant les 2 ans et nous serons informés des résultats du suivi aux échéances prévues par les protocoles d'étude.
Si tout a été mis en œuvre pour mettre au point des vaccins dans les meilleurs délais, toutes les phases habituelles de recherche ont été respectées y compris sur la réalisation des essais cliniques sur plusieurs dizaines de milliers de volontaires à travers le monde.
Ces recherches menées dans les règles de l'art et l'expérience de la vaccination en vie réelle qui a commencé en décembre 2020 sont autant de gages de sécurité du vaccin.
Sources : Sébastien Bruel, Amandine Gagneux-Brunon, Rodolphe Charles, Xavier Gocko, Élisabeth Botelho-Nevers. Développement des vaccins et stratégies vaccinales contre la COVID-19. Des données pour une décision partagée. Médecine. 2021;17(1):4-10. doi:10.1684/med.2021.613
Différents vaccins sont ou seront disponibles dans un avenir proche permettant en cas d’échec d’une stratégie de développement (mauvaise efficacité ou tolérance) d’aboutir au final à un ou plusieurs vaccins sûrs et efficaces. De plus, les données d’efficacité des différentes stratégies vaccinales sur le long terme seront peut être différentes et à prendre en considération dans les années à venir si ce virus venait à s’installer durablement dans la population.
La différence entre ces vaccins repose sur le mécanisme par lequel notre organisme va déclencher une réponse immunitaire contre la protéine présente à la surface du virus (Spike) : premier antigène que notre organisme doit reconnaître. Différents types de vaccins contre la COVID-19 sont en développement :
- les vaccins à virus entiers inactivés
- les vaccins contenant uniquement un fragment du virus : la protéine Spike, produite en laboratoire. Ces vaccins sont appelés vaccins sous-unitaires
- les vaccins qui induisent la production par nos cellules elles-mêmes de la protéine Spike. Ce sont les vaccins à ARNm et les vaccins à vecteur viral
Jusqu'à présent, les vaccins étaient produits à partir de pathogènes (virus ou bactéries) entiers, tués ou inactivés, ou de fragments de ces pathogènes. L'injection de ces pathogènes ou de leurs fragments dans l'organisme permet d'entraîner
une réponse immunitaire.
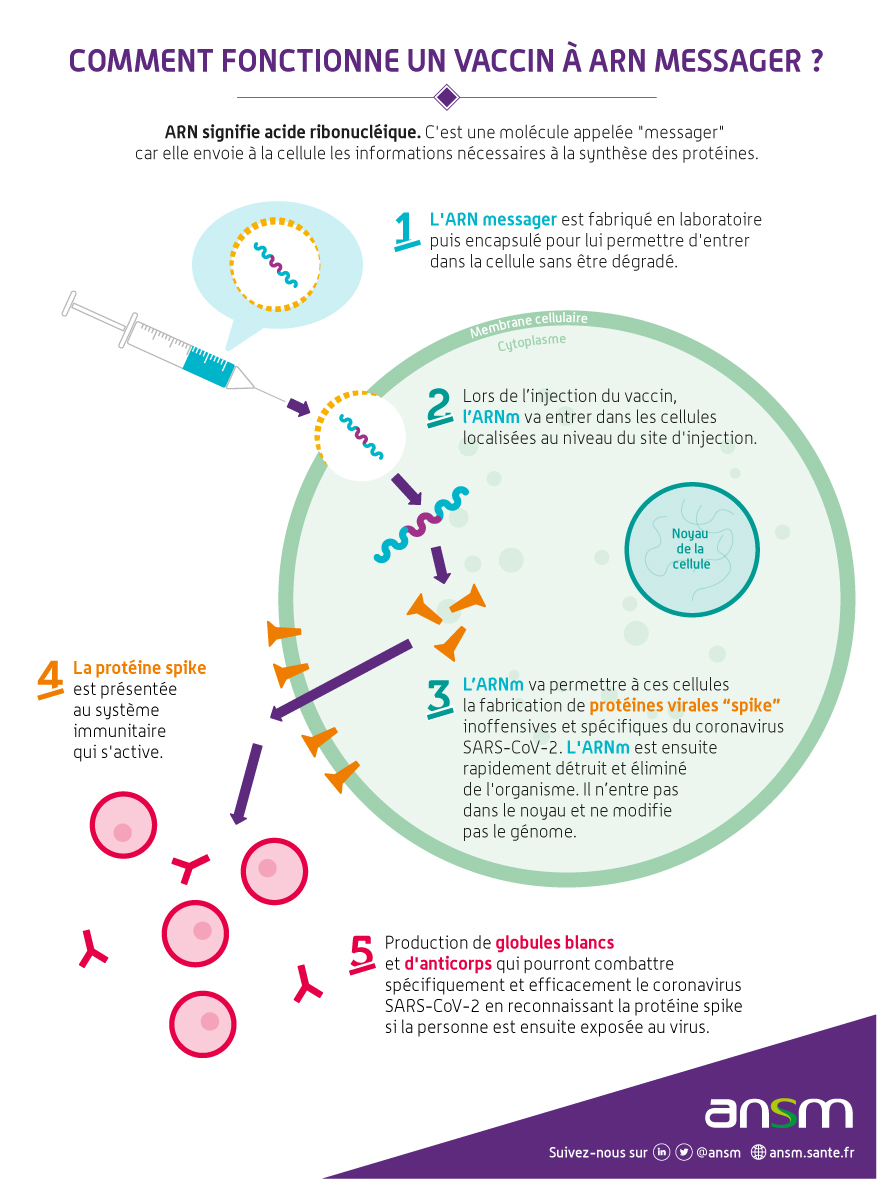
Dans le cas des vaccins à ARNm, le principe est d’injecter des molécules d’ARNm qui codent pour une protéine du SARS-CoV-2 : la protéine Spike. Une fois injectées dans le muscle, ces molécules d'ARNm
vont pouvoir entrer dans les cellules du corps grâce à des nanoparticules lipidiques (la membrane de nos cellules étant elle-même composée de lipides). A l'intérieur des cellules, l'ARN viral introduit va être utilisé pour produire
des protéines, en utilisant le même mécanisme que pour notre propre ARN. Les protéines produites à partir de cet ARN sont reconnues comme étrangères à notre corps, ce qui entraîne une réponse immunitaire. Après avoir été transcrite,
la molécule d'ARN est rapidement détruite.
L’ARN injecté via le vaccin n’a aucun risque de transformer notre génome car il ne pénètre pas dans le noyau des cellules. Or, c’est dans ce noyau cellulaire que se situe notre matériel génétique.
De plus, nos cellules sont incapables de transformer de l'ARN en ADN.
Bien que l'utilisation de l'ARN pour la production d'un vaccin soit inédite chez l'homme, cette technique est déjà utilisée pour le vaccin vétérinaire contre la fièvre porcine.
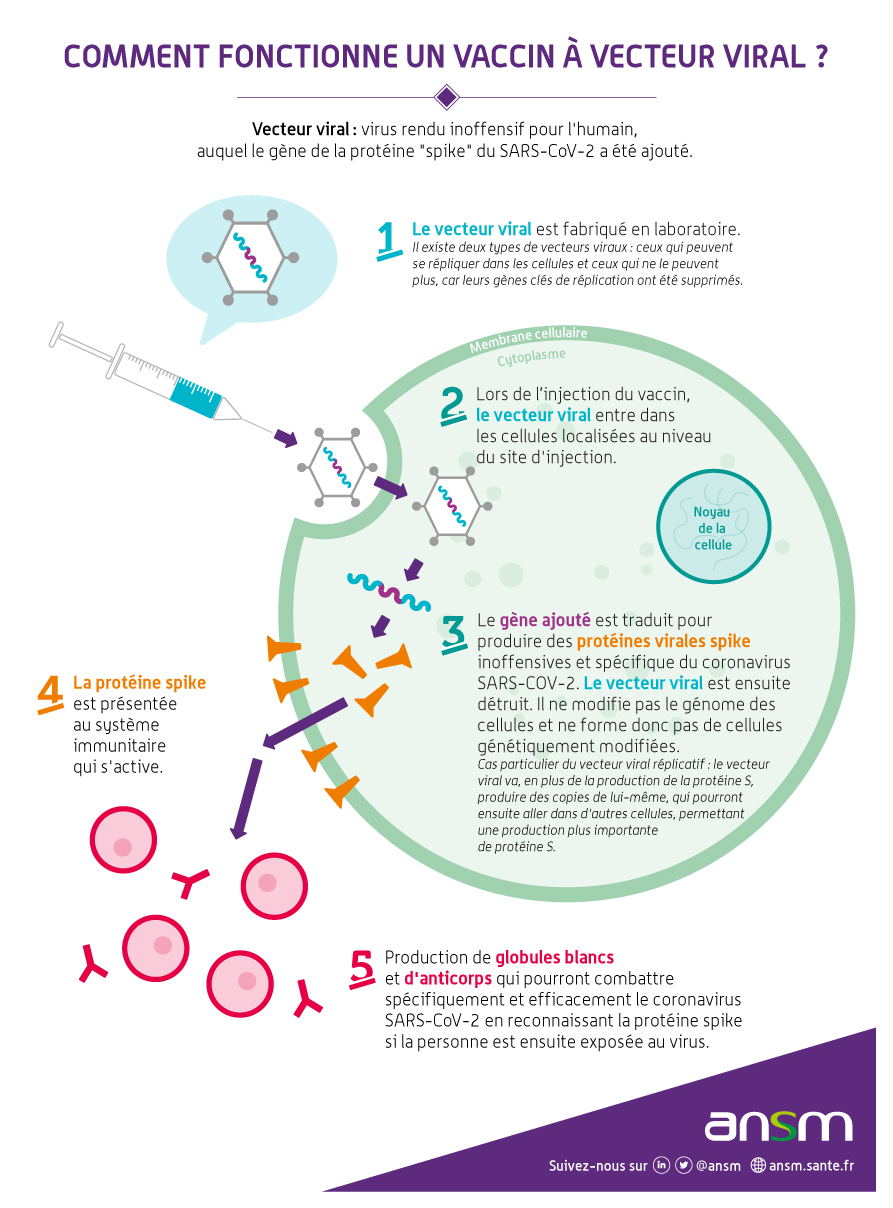
Le mécanisme d’action des vaccins à vecteurs viraux recombinants est connu et a déjà été utilisé pour d’autres vaccins disponibles chez l’homme, tel que le vaccin ERVEBO en prévention de la maladie à virus Ebola. Le vaccin à vecteur viral fonctionne selon le même mécanisme d’action que les vaccins à ARNm. La séquence codant les protéines virales est cependant acheminée à la cellule au moyen d’un vecteur viral, c’est-à-dire un virus modifié et conçu pour transporter la séquence. Il consiste à utiliser un virus initialement peu pathogène et rendu non pathogène et d’intégrer dans son génome la séquence codant la protéine d’intérêt (protéine S dans le cas du SARS-CoV-2).
Un exemple de vaccin disponible est le vaccin AZD1222 d'AstraZeneca. Le vecteur utilisé est le ChAdOx1, un adénovirus de chimpanzé non réplicatif, contenant le gène de la glycoprotéine de surface structurale du SARS-CoV-2, la protéine S, cible de la réponse humorale neutralisante.
La séroprévalence des anticorps contre l’adénovirus de chimpanzé est extrêmement faible chez l’homme et permet ainsi d’éviter une potentielle inefficacité du vaccin AZD1222 liée à une immunité anti-vecteur préexistante.
